TIPOLOGIA DI STUDI E MODULISTICA
Sono di seguito disponibili:
- la documentazione che il promotore e/o lo sperimentatore è tenuto a predisporre per la valutazione di uno studio clinico da parte del Comitato Etico Territoriale Area Sud-Ovest (CET ASOV) o CET nazionale;
- la modulistica centro-specifica che deve essere completata a cura dello sperimentatore locale e trasmessa da quest’ultimo all’Unità Ricerca Clinica dell’Azienda Ulss 9 Scaligera;
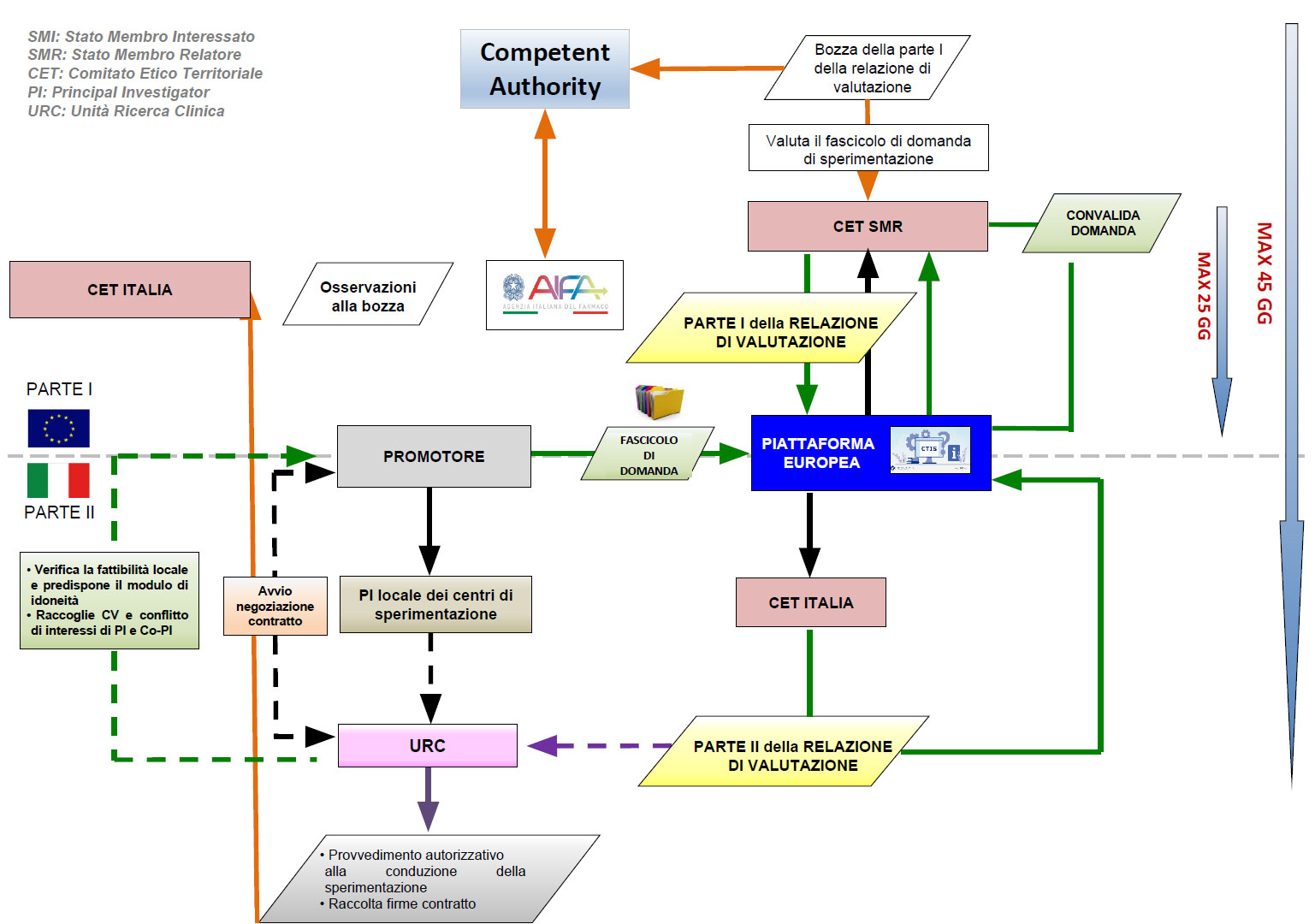
Nel caso di Sperimentazioni Cliniche con Medicinali, queste vengono sottomesse dal Promotore tramite il Clinical Trials Information System (CTIS) secondo quanto previsto dal Regolamento EU 536/2014 e dalle indicazioni presenti sul sito istituzionale di AIFA.
La documentazione da presentare, di competenza del CET, deve essere in linea con quanto previsto nell’Allegato I del Regolamento UE 536/2014 (dalla lettera K alla lettera R).
Per la modulistica da utilizzare bisogna fare riferimento a quanto previsto dal Centro di Coordinamento Nazionale dei Comitati Etici (CCNCE) territoriali per le sperimentazioni cliniche sui medicinali per uso umano e sui dispositivi medici clicca qui. In fase di presentazione dello studio farmacologico sperimentale contattare l’Unità di Ricerca Clinica dell’Ulss 9 per la predisposizione dei seguenti documenti centro-specifici:
- documento di Idoneità Sito Specifica, a firma del:
- Direttore della U.O.C. Assistenza Farmaceutica Territoriale (su delega del Direttore Generale prot.n. 12660 del 03/07/2023 per gli studio condotti in strutture afferenti all’Azienda Ulss 9 Scaligera). Scarica il documento;
- Direttore Ospedale P. Pederzoli Casa di Cura Privata S.p.A., per gli studi condotti presso tale struttura.
- convenzione tra lo Sponsor e l’Azienda Ulss 9 Scaligera.
Per la tipologia di questi studi è previsto il rilascio di un Parere Unico a livello nazionale da parte di uno specifico Comitato Etico Territoriale (CET), che valuterà per tutti i centri partecipanti alla ricerca.
Elenco documenti da presentare ai Comitati Etici della Regione Veneto per il rilascio del Parere Unico valido su tutto il territorio nazionale.
- STUDI OSSERVAZIONALI PROSPETTICI/RETROSPETTIVI FARMACOLOGICI;
- INDAGINE CLINICA CON DISPOSITIVI MEDICI CON MARCATURA CE PER LA DESTINAZIONE D’USO PREVISTA;
- INDAGINE CLINICA CON DISPOSITIVI MEDICI SENZA MARCATURA CE PER LA DESTINAZIONE D’USO PREVISTA.
Modulistica centro Specifica
- Modulo 1 Lettera trasmissione studi altro osservazionali
- Modulo 2 Lettera trasmissione studi con DM
- Modulo 3 Modulo di domanda per indagine clinica PMCF
- Modulo 4 Dichiarazione noprofit DEVICE ALTRO
- Modulo 5 Dichiarazione noprofit DM 30nov21 FARMACI
- Modulo 6 Sinossi in italiano
- Modulo 7 Dichiarazione a cura del Promotore sulla natura Osservazionale
- Modulo 8 Informativa e consenso trattamento dati
- Modulo 9 Modulo di Idoneita sito specifico DM
- Modulo 10 Modulo di fattibilità locale
- Modulo 11 Dichiarazione costi aggiuntivi e compensi sperimentatori
- Modulo 12 Dichiarazione PI osservazionale dispositivo medico
- Modulo 13 Dichiarazione PI osservazionale altro
- Modulo 14 Modulo di domanda per il CE uso compassionevole
- Modulo 15 Esempio Protocollo Uso Terapeutico
- Modulo 16 Lettera di trasmissione emendamento sostanziale
- Modulo 17a Dichiarazione interessi Centro coordinamento Aulss9
- Modulo 17b Dichiarazione interessi Centro coordinamento altri centri
- Modulo 18 CV sperimentatore principale Centro coordinamento
- Modulo 19 Informative pazienti (centro coordinamento)
- Modulo 20 Convenzioni (centro coordinamento)
- Modulo 21 Modello raccolta conservazione uso futuro campioni biologici
- Modulo 22 Documento descrizione misure disposizioni privacy DM e IVD
Altre tipologie di studio (sperimentali s/farmaco e dispositivo, osservazionali s/farmaco e dispositivo, osservazionali con farmaco retrospettivi, studi con IVD)
Le domande di valutazione dovranno essere compilate presentando l’appropriata documentazione ed inviate via mail all’Unità Ricerca Clinica, che ne effettuerà una verifica formale della completezza, e provvederà a sottomettere la pratica alla segreteria del Comitato Etico Territoriale Area Sud-Ovest (CET ASOV), per la valutazione dello studio nella prima seduta utile:
Elenco documenti da presentare all’URC:
- STUDIO SPERIMENTALE SENZA FARMACO E DISPOSITIVO;
- STUDIO OSSERVAZIONALE SENZA FARMACO E DISPOSITIVO;
- STUDIO CON IVD.
Modulistica centro Specifica
- Modulo 1 Lettera trasmissione studi altro osservazionali
- Modulo 2 Lettera trasmissione studi con DM
- Modulo 3 Modulo di domanda per indagine clinica PMCF
- Modulo 4 Dichiarazione noprofit DEVICE ALTRO
- Modulo 5 Dichiarazione noprofit DM 30nov21 FARMACI
- Modulo 6 Sinossi in italiano
- Modulo 7 Dichiarazione a cura del Promotore sulla natura Osservazionale
- Modulo 8 Informativa e consenso trattamento dati
- Modulo 9 Modulo di Idoneita sito specifico DM
- Modulo 10 Modulo di fattibilità locale
- Modulo 11 Dichiarazione costi aggiuntivi e compensi sperimentatori
- Modulo 12 Dichiarazione PI osservazionale dispositivo medico
- Modulo 13 Dichiarazione PI osservazionale altro
- Modulo 14 Modulo di domanda per il CE uso compassionevole
- Modulo 15 Esempio Protocollo Uso Terapeutico
- Modulo 16 Lettera di trasmissione emendamento sostanziale
- Modulo 17a Dichiarazione interessi Centro coordinamento Aulss9
- Modulo 17b Dichiarazione interessi Centro coordinamento altri centri
- Modulo 18 CV sperimentatore principale Centro coordinamento
- Modulo 19 Informative pazienti (centro coordinamento)
- Modulo 20 Convenzioni (centro coordinamento)
- Modulo 21 Modello raccolta conservazione uso futuro campioni biologici
- Modulo 22 Documento descrizione misure disposizioni privacy DM e IVD
Le domande di emendamento sostanziale dovranno essere compilate ed inviate via mail all’Unità di Ricerca Clinica, che provvederà verificare la correttezza e la completezza, e a sottomettere la pratica alla Segreteria del CET entro la deadline prevista dal Calendario Riunioni.
Il Centro sede della ricerca NON è una struttura afferente al CET:
La sottomissione avverrà per mezzo del Promotore.
EMENDAMENTO NON SOSTANZIALE
Il centro sede della ricerca è una struttura afferente al CET:
Le richieste dovranno pervenire tramite mail all’Unità di Ricerca Clinica, che si occuperà di inviarle al CET per presa visione.
Il Centro sede della ricerca NON è una struttura afferente al CET:
La sottomissione avverrà per mezzo del Promotore. Il Centro sede della ricerca NON è una struttura afferente al CET: La sottomissione avverrà per mezzo del Promotore.
Altre informazioni
- Comunicazioni relative al MONITORAGGIO dello studio (notifica arruolamento primo paziente, stato di avanzamento locale, dichiarazione di avvio studio, relazione di chiusura studio);
- Comunicazione relative a modifiche della fattibilità locale (modifica al budget, modifica alla fattibilità, proroghe comodati d’uso);
I documenti dovranno pervenire tramite mail al’URC, che si occuperà di inviarli al CET per presa visione, previa verifica della documentazione.
Il CET ASOV valuta le richieste di Uso Terapeutico di Medicinale Sottoposto a Sperimentazione Clinica secondo il DM 07/09/2017.
Le domande di valutazione vanno inviate direttamente all'Ufficio di Segreteria Tecnico-Scientifica del CET email: comitatoetico@aovr.veneto.it

